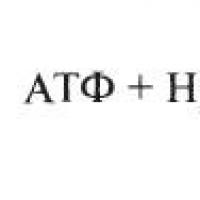ATP'nin hidrolizi sonucunda AmphADP oluşur. ATF: enerji para birimi. Oksidatif dekarboksilasyon - piruvatın asetil-CoA'ya oksidasyonu, yapısal olarak çoklu enzim sisteminde birleştirilen bir dizi enzim ve koenzimin katılımıyla meydana gelir, elde edilir
ATP (adenozin trifosfat)– başta hücrelere enerji sağlamak olmak üzere bir dizi biyokimyasal süreçte önemli bir rol oynayan nükleosid trifosfatlar grubundan organik bir bileşik.
Makale navigasyonu
ATP'nin yapısı ve sentezi
Adenozin trifosfat, üç molekül ortofosforik asidin bağlandığı adenindir. Adenin, nükleik asitler de dahil olmak üzere canlı doğada yaygın olarak bulunan diğer birçok bileşiğin bir parçasıdır.
Vücut tarafından çeşitli amaçlarla kullanılan enerjinin salınması, ATP'nin hidrolizi sırasında meydana gelir ve bir veya iki serbest fosforik asit molekülünün ortaya çıkmasına yol açar. İlk durumda, adenosin trifosfat, adenosin difosfata (ADP), ikincisinde ise adenosin monofosfata (AMP) dönüştürülür.
Adenozin difosfatın fosforik asit ile kombinasyonu nedeniyle canlı bir organizmada meydana gelen ATP sentezi çeşitli şekillerde gerçekleşebilir:
- Ana: organik maddelerin oksidasyonu sırasında hücre içi organellerde - mitokondride meydana gelen oksidatif fosforilasyon.
- İkinci yol: sitoplazmada meydana gelen ve anaerobik işlemlerde merkezi bir rol oynayan substrat fosforilasyonu.
ATP'nin İşlevleri
Adenozin trifosfat enerji depolamada önemli bir rol oynamaz, bunun yerine hücresel enerji metabolizmasında taşıma fonksiyonlarını yerine getirir. Adenozin trifosfat ADP'den sentezlenir ve kısa sürede tekrar ADP'ye dönüştürülerek yararlı enerji açığa çıkar.
Omurgalılarda ve insanlarda ATP'nin temel işlevi kas liflerinin motor aktivitesini sağlamaktır.
Eforun süresine bağlı olarak, ister kısa süreli iş, ister uzun süreli (döngüsel) yük olsun, enerji süreçleri oldukça farklıdır. Ancak hepsinde adenozin trifosfat çok önemli bir rol oynuyor.
ATP yapısal formülü:
Adenozin trifosfat, enerji fonksiyonunun yanı sıra sinir hücreleri arasındaki sinyal iletiminde ve diğer hücreler arası etkileşimlerde, enzimlerin ve hormonların etkisinin düzenlenmesinde önemli bir rol oynar. Protein sentezinin başlangıç ürünlerinden biridir.
Glikoliz ve oksidasyon sırasında kaç ATP molekülü üretilir?
Bir molekülün ömrü genellikle bir dakikadan fazla değildir, bu nedenle herhangi bir anda bu maddenin bir yetişkinin vücudundaki içeriği yaklaşık 250 gramdır. Günde sentezlenen toplam Adenozin Trifosfat miktarının genellikle vücudun kendi ağırlığıyla karşılaştırılabilir olmasına rağmen.
Glikoliz süreci 3 aşamada gerçekleşir:
- Hazırlık.
Bu aşamanın girişinde adenozin trifosfat molekülleri oluşmaz. - Anaerobik.
2 ATP molekülü oluşur. - Aerobik.
Bu sırada PVC ve piruvik asidin oksidasyonu meydana gelir. 1 glikoz molekülünden 36 ATP molekülü oluşur.
Toplamda, 1 glikoz molekülünün glikolizi sırasında 38 ATP molekülü oluşur: 2'si glikolizin anaerobik aşamasında, 36'sı piruvik asidin oksidasyonu sırasında.
Şekilde iki yöntem gösterilmektedir ATP yapısı görselleri. Adenozin monofosfat (AMP), adenozin difosfat (ADP) ve adenozin trifosfat (ATP), nükleotidler adı verilen bir bileşik sınıfına aittir. Nükleotid molekülü beş karbonlu şeker, azotlu bir baz ve fosforik asitten oluşur. AMP molekülünde şeker ribozla, baz ise adeninle temsil edilir. ADP molekülünde iki, ATP molekülünde üç fosfat grubu vardır.
ATP değeri
ATP ADP'ye bölündüğünde ve inorganik fosfat (Pn) enerjisi açığa çıkar:
Reaksiyon suyun emilmesiyle gerçekleşir yani hidrolizi temsil eder (makalemizde bu çok yaygın biyokimyasal reaksiyon türüyle birçok kez karşılaştık). ATP'den ayrılan üçüncü fosfat grubu hücrede inorganik fosfat (Pn) halinde kalır. Bu reaksiyon için serbest enerji verimi, 1 mol ATP başına 30,6 kJ'dir.
ADF'den ve fosfat, ATP yeniden sentezlenebilir ancak bu, yeni oluşan ATP'nin 1 mol'ü başına 30,6 kJ enerji harcanmasını gerektirir.
Bu reaksiyonda yoğunlaşma reaksiyonu olarak adlandırılan reaksiyonda su açığa çıkar. ADP'ye fosfat eklenmesine fosforilasyon reaksiyonu denir. Yukarıdaki her iki denklem birleştirilebilir:

Bu geri dönüşümlü reaksiyon, adı verilen bir enzim tarafından katalize edilir. ATPaz.
Daha önce de belirtildiği gibi, tüm hücrelerin işlerini gerçekleştirmek için enerjiye ihtiyacı vardır ve herhangi bir organizmanın tüm hücreleri için bu enerjinin kaynağı ATP olarak görev yapar. Bu nedenle ATP'ye hücrelerin "evrensel enerji taşıyıcısı" veya "enerji para birimi" adı verilir. Uygun bir benzetme elektrikli pillerdir. Bunları neden kullanmadığımızı unutmayın. Onların yardımıyla bir durumda ışığı, diğer durumda sesi alabiliriz, bazen mekanik hareket, bazen de onlardan elektrik enerjisine ihtiyaç duyarız. Pillerin rahatlığı, aynı enerji kaynağını (pil) nereye koyduğumuza bağlı olarak çeşitli amaçlar için kullanabilmemizdir. ATP hücrelerde aynı rolü oynar. Kas kasılması, sinir uyarılarının iletilmesi, maddelerin aktif taşınması veya protein sentezi ve diğer tüm hücresel aktivite türleri gibi çeşitli işlemler için enerji sağlar. Bunu yapmak için hücre aparatının ilgili kısmına basitçe "bağlanması" gerekir.
Analojiye devam edilebilir. İlk önce pillerin yapılması gerekiyor ve bunlardan bazıları (şarj edilebilir olanlar) tıpkı şarj edilebilir. Piller bir fabrikada üretildiğinde, belirli bir miktarda enerjinin pillerde depolanması (ve dolayısıyla fabrika tarafından tüketilmesi) gerekir. ATP sentezi de enerji gerektirir; Kaynağı, solunum sırasında organik maddelerin oksidasyonudur. ADP'yi fosforile etmek için oksidasyon işlemi sırasında enerji açığa çıktığı için, bu tür fosforilasyona oksidatif fosforilasyon denir. Fotosentez sırasında ışık enerjisinden ATP üretilir. Bu işleme fotofosforilasyon denir (bkz. Bölüm 7.6.2). Hücrede ayrıca ATP'nin çoğunu üreten "fabrikalar" da vardır. Bunlar mitokondri; aerobik solunum sırasında ATP'nin oluşturulduğu kimyasal "montaj hatları" içerirler. Son olarak, boşalan "piller" de hücrede yeniden şarj edilir: İçinde bulunan enerjiyi serbest bırakan ATP, ADP ve Fn'ye dönüştürüldükten sonra, süreçte alınan enerji nedeniyle ADP ve Fn'den hızlı bir şekilde tekrar sentezlenebilir. Organik maddenin yeni kısımlarının oksidasyonundan kaynaklanan solunum.
ATP miktarı Herhangi bir anda hücrede bulunan miktar çok küçüktür. Bu nedenle ATF'de deposunu değil, yalnızca enerji taşıyıcısını görmelisiniz. Uzun süreli enerji depolamak için yağlar veya glikojen gibi maddeler kullanılır. Hücreler ATP seviyelerine karşı çok duyarlıdır. Kullanım oranı arttıkça bu seviyeyi koruyan nefes alma işleminin hızı da artar.
ATP'nin Rolü Hücresel solunum ile enerji tüketimini içeren süreçler arasında bağlantı kuran bir bağlantı olan bu şema, basit gibi görünse de çok önemli bir modeli göstermektedir.
Bu nedenle genel olarak nefes almanın işlevinin olduğu söylenebilir. ATP üretmek.

Yukarıda söylenenleri kısaca özetleyelim.
1. ADP'den ve inorganik fosfattan ATP sentezi, 1 mol ATP başına 30,6 kJ enerji gerektirir.
2. ATP tüm canlı hücrelerde mevcuttur ve bu nedenle evrensel bir enerji taşıyıcısıdır. Başka hiçbir enerji taşıyıcısı kullanılmaz. Bu, işleri basitleştirir; gerekli hücresel aparatlar daha basit olabilir ve daha verimli ve ekonomik şekilde çalışabilir.
3. ATP, enerji gerektiren herhangi bir işlem için hücrenin herhangi bir kısmına kolayca enerji iletir.
4. ATP hızla enerjiyi serbest bırakır. Bu sadece bir reaksiyon gerektirir - hidroliz.
5. ADP ve inorganik fosfattan ATP üretim hızı (solunum işlem hızı) ihtiyaca göre kolaylıkla ayarlanabilir.
6. ATP, glikoz gibi organik maddelerin oksidasyonu sırasında açığa çıkan kimyasal enerji nedeniyle solunum sırasında, güneş enerjisi nedeniyle fotosentez sırasında sentezlenir. ADP ve inorganik fosfattan ATP oluşumuna fosforilasyon reaksiyonu denir. Fosforilasyon enerjisi oksidasyonla sağlanıyorsa, oksidatif fosforilasyondan söz ederiz (bu işlem solunum sırasında meydana gelir), ancak fosforilasyon için ışık enerjisi kullanılıyorsa, o zaman işleme fotofosforilasyon denir (bu, fotosentez sırasında meydana gelir).
İyi çalışmanızı bilgi tabanına göndermek basittir. Aşağıdaki formu kullanın
Bilgi tabanını çalışmalarında ve çalışmalarında kullanan öğrenciler, lisansüstü öğrenciler, genç bilim insanları size çok minnettar olacaklardır.
Yayınlanan http://www.allbest.ru/
- giriiş
- 1.1 ATP'nin kimyasal özellikleri
- 1.2 ATP'nin fiziksel özellikleri
- 2.1
- 3.1 Hücredeki rol
- 3.2 Enzim fonksiyonundaki rol
- 3.4 ATP'nin diğer işlevleri
- Çözüm
- Kaynakça
Sembollerin listesi
ATP - adenosin trifosfat
ADP - adenozin difosfat
AMP - adenozin monofosfat
RNA - ribonükleik asit
DNA - deoksiribonükleik asit
NAD - nikotinamid adenin dinükleotidi
PVC - pirüvik asit
G-6-P - fosfoğlukoz izomeraz
F-6-F - fruktoz-6-fosfat
TPP - tiamin pirofosfat
FAD - feniladenin dinükleotid
Fn - sınırsız fosfat
G - entropi
RNR - ribonükleotid redüktaz
giriiş
Gezegenimizde yaşayan tüm canlılar için ana enerji kaynağı, yalnızca yeşil bitki, alg, yeşil ve mor bakteri hücreleri tarafından doğrudan kullanılan güneş ışığının enerjisidir. Bu hücrelerde fotosentez işlemi sırasında karbondioksit ve sudan organik maddeler (karbonhidratlar, yağlar, proteinler, nükleik asitler vb.) oluşur. Hayvanlar bitkileri yiyerek organik maddeleri bitmiş halde elde ederler. Bu maddelerde depolanan enerji, onlarla birlikte heterotrofik organizmaların hücrelerine geçer.
Hayvan organizmalarının hücrelerinde organik bileşiklerin oksidasyonu sırasındaki enerjisi ATP enerjisine dönüştürülür. (Bu durumda açığa çıkan karbondioksit ve su, yine ototrofik organizmalar tarafından fotosentez işlemleri için kullanılır.) Tüm hayati işlemler ATP'nin enerjisi kullanılarak gerçekleştirilir: organik bileşiklerin biyosentezi, hareket, büyüme, hücre bölünmesi vb.
ATP'nin vücutta oluşumu ve kullanımı konusu uzun zamandır yeni değil, ancak hem tek bir kaynakta hem de daha az sıklıkla bu süreçlerin her ikisinin de aynı anda bir analizini tam bir tartışmayı bulmanız nadirdir ve farklı organizmalarda.
Bu bağlamda, çalışmamızın önemi canlı organizmalarda ATP'nin oluşumu ve kullanımına ilişkin kapsamlı bir çalışma haline geldi, çünkü bu konu popüler bilim literatüründe uygun düzeyde çalışılmamaktadır.
Çalışmamızın amacı şuydu:
· Hayvan ve insan vücudunda ATP'nin oluşum mekanizmalarının ve kullanım yollarının incelenmesi.
Bize aşağıdaki görevler verildi:
· ATP'nin kimyasal yapısını ve özelliklerini inceleyin;
· Canlı organizmalarda ATP oluşumunun yollarını analiz etmek;
· Canlı organizmalarda ATP'yi kullanmanın yollarını düşünün;
· ATP'nin insan vücudu ve hayvanlar için önemini düşünün.
Bölüm 1. ATP'nin kimyasal yapısı ve özellikleri
1.1 ATP'nin kimyasal özellikleri
Adenozin trifosfat, organizmalarda enerji ve madde metabolizmasında son derece önemli bir rol oynayan bir nükleotiddir; Her şeyden önce bileşiğin, canlı sistemlerde meydana gelen tüm biyokimyasal süreçler için evrensel bir enerji kaynağı olduğu bilinmektedir. ATP, 1929'da Karl Lohmann tarafından keşfedildi ve 1941'de Fritz Lipmann, ATP'nin hücredeki ana enerji taşıyıcısı olduğunu gösterdi.
ATP'nin sistematik adı:
9-in-D-ribofuranosiladenin-5"-trifosfat, veya
9-in-D-ribofuranosil-6-amino-purin-5"-trifosfat.
Kimyasal olarak ATP, adenin ve ribozun bir türevi olan adenosinin trifosfat esteridir.
Pürin azotlu bazı - adenin - ribozun 1" karbonuna bir β-N-glikosidik bağ ile bağlanır. Üç fosforik asit molekülü, sırasıyla aşağıdaki harflerle gösterilen, ribozun 5" karbonuna sırayla bağlanır: b, c ve d.
ATP'nin yapısı RNA'nın bir parçası olan adenin nükleotidine benzer, ancak bir fosforik asit yerine ATP üç fosforik asit kalıntısı içerir. Hücreler gözle görülür miktarlarda asitleri değil, yalnızca tuzlarını içerebilir. Bu nedenle fosforik asit ATP'ye bir kalıntı olarak girer (asitin OH grubu yerine negatif yüklü bir oksijen atomu vardır).
Enzimlerin etkisi altında, ATP molekülü kolayca hidrolize uğrar, yani bir su molekülüne bağlanır ve adenozin difosforik asit (ADP) oluşturmak üzere parçalanır:
ATP + H2O ADP + H3PO4.
Başka bir fosforik asit kalıntısının ortadan kaldırılması, ADP'yi adenozin monofosforik asit AMP'ye dönüştürür:
ADP + H2O AMP + H3PO4.
Bu reaksiyonlar tersine çevrilebilir, yani AMP, ADP'ye ve ardından ATP'ye dönüşerek enerji biriktirebilir. Düzenli bir peptid bağının kırılması yalnızca 12 kJ/mol enerji açığa çıkarır. Fosforik asit kalıntılarını bağlayan bağlar da yüksek enerjilidir (bunlara yüksek enerji de denir): her birinin yok edilmesi 40 kJ/mol enerji açığa çıkarır. Bu nedenle ATP, evrensel bir biyolojik enerji akümülatörü olarak hücrelerde merkezi bir rol oynar. ATP molekülleri mitokondri ve kloroplastlarda sentezlenir (sitoplazmada sadece küçük bir miktar sentezlenir) ve daha sonra hücrenin çeşitli organellerine giderek tüm hayati süreçler için enerji sağlar.
ATP'nin enerjisi nedeniyle hücre bölünmesi meydana gelir, maddelerin hücre zarları boyunca aktif taşınması, sinir uyarılarının iletimi sırasında zarın elektrik potansiyelinin korunmasının yanı sıra yüksek moleküler bileşiklerin biyosentezi ve fiziksel çalışma meydana gelir.
Artan yük ile (örneğin kısa mesafeli koşularda), kaslar yalnızca ATP tedariki nedeniyle çalışır. Kas hücrelerinde bu rezerv birkaç düzine kasılma için yeterlidir ve ardından ATP miktarının yenilenmesi gerekir. ADP ve AMP'den ATP sentezi, karbonhidratların, lipitlerin ve diğer maddelerin parçalanması sırasında açığa çıkan enerji nedeniyle oluşur. Zihinsel çalışma yapmak aynı zamanda büyük miktarda ATP gerektirir. Bu nedenle zihinsel çalışması olan kişiler, parçalanması ATP sentezini sağlayan artan miktarda glikoza ihtiyaç duyar.
1.2 ATP'nin fiziksel özellikleri
ATP, adenozin ve ribozdan ve üç fosfat grubundan oluşur. ATP suda oldukça çözünür ve pH 6,8-7,4'teki çözeltilerde oldukça stabildir, ancak aşırı pH'da hızla hidrolize edilir. Bu nedenle ATP en iyi şekilde susuz tuzlarda depolanır.
ATP kararsız bir moleküldür. Tamponlanmamış suda ADP ve fosfata hidrolize olur. Bunun nedeni, ATP'deki fosfat grupları arasındaki bağların gücünün, ürünleri (ADP + fosfat) ile su arasındaki hidrojen bağlarının (hidrasyon bağları) gücünden daha az olmasıdır. Dolayısıyla ATP ve ADP suda kimyasal dengedeyse, ATP'nin neredeyse tamamı sonunda ADP'ye dönüştürülecektir. Dengeden uzak bir sistem Gibbs serbest enerjisini içerir ve iş yapabilir. Canlı hücreler, ATP'nin ADP'ye oranını, ADP konsantrasyonundan bin kat daha yüksek bir ATP konsantrasyonuyla, dengeden on büyüklük düzeyinde bir noktada tutar. Denge konumundan bu kayma, hücredeki ATP'nin hidrolizinin büyük miktarda serbest enerji açığa çıkardığı anlamına gelir.
Bir ATP molekülündeki iki yüksek enerjili fosfat bağı (bitişik fosfatları birbirine bağlayanlar), o molekülün yüksek enerji içeriğinden sorumludur. ATP'de depolanan enerji hidroliz yoluyla serbest bırakılabilir. Riboz şekerinin distalinde bulunan g-fosfat grubu, b- veya b-fosfattan daha yüksek bir hidroliz enerjisine sahiptir. Bir ATP kalıntısının hidrolizi veya fosforilasyonundan sonra oluşan bağların enerjisi diğer ATP bağlarından daha düşüktür. Enzim katalizli ATP hidrolizi veya ATP fosforilasyonu sırasında, mevcut serbest enerji, canlı sistemler tarafından iş yapmak için kullanılabilir.
Potansiyel olarak reaktif moleküllerden oluşan herhangi bir kararsız sistem, hücrelerin konsantrasyonlarını reaksiyonun denge noktasından uzakta tutması durumunda potansiyel olarak serbest enerjiyi depolamanın bir yolu olarak hizmet edebilir. Bununla birlikte, çoğu polimerik biyomolekülde olduğu gibi, RNA, DNA ve ATP'nin basit monomerlere parçalanması, hem enerji hem de entropi salınımını içerir; bu da hem standart konsantrasyon hem de hücrede bulunan konsantrasyonlarla ilgili hususları artırır.
ATP hidrolizi sonucunda açığa çıkan standart enerji miktarı, doğal (standart) koşullarla ilişkili olmayan enerjideki değişikliklerden ve ardından biyolojik konsantrasyonun düzeltilmesinden hesaplanabilir. ATP'nin ADP'ye ve inorganik fosfatlara ayrışması için standart sıcaklık ve basınçta termal enerjideki (entalpi) net değişim 20,5 kJ/mol'dür ve serbest enerji değişimi 3,4 kJ/mol'dür. Durum standardı 1 M'de ATP'den fosfat veya pirofosfatın parçalanmasıyla açığa çıkan enerji:
ATP + H 2 O > ADP + P i DG ? = - 30,5 kJ/mol (-7,3 kcal/mol)
ATP + H 2 O > AMP + PP i DG ? = - 45,6 kJ/mol (-10,9 kcal/mol)
Bu değerler, fizyolojik koşullar ve hücresel ATP/ADP altındaki enerji değişikliklerini hesaplamak için kullanılabilir. Bununla birlikte, enerji yükü adı verilen daha temsili bir önem daha sık işe yarar. Gibbs serbest enerjisi için değerler verilmiştir. Bu reaksiyonlar, toplam iyon kuvveti ve Mg2+ ve Ca2+ iyonları gibi alkalin toprak metallerinin varlığı dahil olmak üzere bir dizi faktöre bağlıdır. Normal koşullar altında DG yaklaşık -57 kJ/mol'dür (-14 kcal/mol).
protein biyolojik pil enerjisi
Bölüm 2. ATP oluşumunun yolları
Vücutta ATP, ADP'nin fosforilasyonuyla sentezlenir:
ADP + H3PO4 + enerji> ATP + H 2 O.
ADP'nin fosforilasyonu iki şekilde mümkündür: substrat fosforilasyonu ve oksidatif fosforilasyon (oksitleyici maddelerin enerjisini kullanarak). ATP'nin büyük kısmı, H'ye bağımlı ATP sentaz tarafından oksidatif fosforilasyon sırasında mitokondriyal membranlarda oluşturulur. ATP'nin substrat fosforilasyonu, membran enzimlerinin katılımını gerektirmez; glikoliz sırasında veya bir fosfat grubunun diğer yüksek enerjili bileşiklerden aktarılmasıyla gerçekleşir.
ADP'nin fosforilasyonu ve ardından ATP'nin bir enerji kaynağı olarak kullanılması reaksiyonları, enerji metabolizmasının özü olan döngüsel bir süreç oluşturur.
ATP vücutta en sık yenilenen maddelerden biridir. Yani insanlarda bir ATP molekülünün ömrü 1 dakikadan azdır. Gün boyunca, bir ATP molekülü ortalama 2000-3000 döngü yeniden sentezden geçer (insan vücudu günde yaklaşık 40 kg ATP sentezler), yani vücutta neredeyse hiç ATP rezervi oluşturulmaz ve normal yaşam için Sürekli olarak yeni ATP moleküllerinin sentezlenmesi gerekir.
Oksidatif fosforilasyon -
Bununla birlikte, karbonhidratlar çoğunlukla substrat olarak kullanılır. Bu nedenle beyin hücreleri, karbonhidratlardan başka herhangi bir substratı beslenme için kullanamaz.
Kompleks öncesi karbonhidratlar basit karbonhidratlara parçalanarak glikoz oluşumuna yol açar. Glikoz, hücresel solunum sürecinde evrensel bir substrattır. Glikoz oksidasyonu 3 aşamaya ayrılır:
1. glikoliz;
2. Oksidatif dekarboksilasyon ve Krebs döngüsü;
3. oksidatif fosforilasyon.
Bu durumda glikoliz, aerobik ve anaerobik solunum için ortak bir aşamadır.
2 .1.1 GlicoLiz- ATP sentezinin eşlik ettiği, hücrelerde glikozun sıralı parçalanmasının enzimatik bir süreci. Aerobik koşullar altında glikoliz, piruvik asit (piruvat) oluşumuna yol açar, anaerobik koşullar altında glikoliz, laktik asit (laktat) oluşumuna yol açar. Glikoliz, hayvanlarda glikoz katabolizmasının ana yoludur.
Glikolitik yol, her biri ayrı bir enzim tarafından katalize edilen 10 ardışık reaksiyondan oluşur.
Glikoliz süreci iki aşamaya ayrılabilir. 2 ATP molekülünün enerji tüketimiyle oluşan ilk aşama, bir glikoz molekülünün 2 molekül gliseraldehit-3-fosfata bölünmesinden oluşur. İkinci aşamada, ATP sentezinin eşlik ettiği gliseraldehit-3-fosfatın NAD'a bağlı oksidasyonu meydana gelir. Glikolizin kendisi tamamen anaerobik bir işlemdir, yani reaksiyonların meydana gelmesi için oksijenin varlığına gerek yoktur.
Glikoliz hemen hemen tüm canlı organizmalarda bilinen en eski metabolik süreçlerden biridir. Muhtemelen glikoliz, ilkel prokaryotlarda 3,5 milyar yıldan fazla bir süre önce ortaya çıktı.
Glikolizin sonucu, bir glikoz molekülünün iki molekül piruvik asite (PVA) dönüştürülmesi ve koenzim NADH formunda iki indirgeyici eşdeğerin oluşmasıdır.
Glikolizin tam denklemi şöyledir:
C6H1206 + 2NAD + + 2ADP + 2P n = 2NAD H + 2PVK + 2ATP + 2H20 + 2H +.
Hücrede oksijen yokluğunda veya eksikliğinde piruvik asit laktik asite indirgenir, bu durumda glikolizin genel denklemi aşağıdaki gibi olacaktır:
C6H1206 + 2ADP + 2P n = 2 laktat + 2ATP + 2H20.
Bu nedenle, bir glikoz molekülünün anaerobik parçalanması sırasında, toplam net ATP verimi, ADP'nin substrat fosforilasyon reaksiyonlarında elde edilen iki moleküldür.
Aerobik organizmalarda glikolizin son ürünleri, hücresel solunumla ilgili biyokimyasal döngülerde daha ileri dönüşümlere uğrar. Sonuç olarak, hücresel solunumun son aşamasında bir glikoz molekülünün tüm metabolitlerinin tamamen oksidasyonundan sonra - oksijen varlığında mitokondriyal solunum zincirinde meydana gelen oksidatif fosforilasyon - her glikoz için ek 34 veya 36 ATP molekülü sentezlenir. molekül.
Glikolizin ilk reaksiyonu, dokuya özgü enzim heksokinazın 1 molekül ATP'nin enerji harcamasıyla katılımıyla ortaya çıkan bir glikoz molekülünün fosforilasyonudur; aktif glikoz formu oluşur - glikoz-6-fosfat (G-6-F):
Reaksiyonun gerçekleşmesi için ortamda ATP molekülünün karmaşık bir şekilde bağlandığı Mg2+ iyonlarının varlığı gereklidir. Bu reaksiyon geri döndürülemez ve ilk anahtar reaksiyon glikoliz.
Glikozun fosforilasyonunun iki amacı vardır: Birincisi, nötr glikoz molekülünü geçirgen olan plazma zarının negatif yüklü G-6-P moleküllerinin geçmesine izin vermemesi nedeniyle fosforile edilmiş glikoz hücre içinde kilitlenir. İkincisi, fosforilasyon sırasında glikoz, biyokimyasal reaksiyonlara katılabilecek ve metabolik döngülere dahil olabilecek aktif bir forma dönüştürülür.
Heksokinazın hepatik izoenzimi olan glukokinaz, kan şekeri seviyelerinin düzenlenmesinde önemlidir.
Bir sonraki reaksiyonda ( 2 ) fosfoğlukoizomeraz G-6-P enzimi tarafından dönüştürülür fruktoz 6-fosfat (F-6-F):
Bu reaksiyon için enerjiye gerek yoktur ve reaksiyon tamamen geri dönüşümlüdür. Bu aşamada fruktoz da fosforilasyon yoluyla glikoliz sürecine dahil edilebilir.
Daha sonra neredeyse hemen birbirini takip eden iki reaksiyon gelir: fruktoz-6-fosfatın geri dönüşümsüz fosforilasyonu ( 3 ) ve sonuçta ortaya çıkan geri dönüşümlü aldol bölünmesi fruktoz 1,6-bifosfat (F-1.6-bF) iki üçlüye ( 4 ).
P-6-P'nin fosforilasyonu, başka bir ATP molekülünün enerjisinin harcanmasıyla fosfofruktokinaz tarafından gerçekleştirilir; bu ikinci anahtar reaksiyon glikoliz, onun düzenlenmesi bir bütün olarak glikolizin yoğunluğunu belirler.
Aldol bölünmesi F-1.6-bF fruktoz-1,6-bisfosfat aldolazın etkisi altında oluşur:
Dördüncü reaksiyonun sonucunda; dihidroksiaseton fosfat Ve gliseraldehit-3-fosfat ve ilki neredeyse anında etki altına giriyor fosfotrioz izomeraz ikinciye gider ( 5 ), daha fazla dönüşüme katılan:
Her bir gliseraldehit fosfat molekülü, varlığında NAD+ tarafından oksitlenir. dehidrojenazlar gliseraldehit fosfatönce 1,3- Dvefosfoglis- oran (6 ):
Sonraki ile 1,3-difosfogliserat 1. pozisyonda yüksek enerjili bir bağ içeren fosfogliserat kinaz enzimi, bir fosforik asit kalıntısını ADP molekülüne aktarır (reaksiyon 7 ) - bir ATP molekülü oluşur:
Bu substrat fosforilasyonunun ilk reaksiyonudur. Bu andan itibaren, ilk aşamanın enerji maliyetleri telafi edildiğinden, glikoz parçalama süreci enerji açısından kârsız olmaktan çıkar: harcanan iki yerine 2 ATP molekülü sentezlenir (her 1,3-difosfogliserat için bir tane). tepkiler 1 Ve 3 . Bu reaksiyonun gerçekleşmesi için sitozolde ADP'nin bulunması gerekir, yani hücrede ATP fazlalığı (ve ADP eksikliği) olduğunda hızı düşer. Metabolize edilmeyen ATP hücrede birikmediği ve basitçe yok edildiği için bu reaksiyon glikolizin önemli bir düzenleyicisidir.
Daha sonra sırayla: fosfogliserol mutaz formları 2-fosfo- gliserat (8 ):
Enolaz formları fosfoenolpiruvat (9 ):
Son olarak, ADP'nin substrat fosforilasyonunun ikinci reaksiyonu, piruvat ve ATP'nin enol formunun oluşmasıyla meydana gelir ( 10 ):
Reaksiyon piruvat kinazın etkisi altında meydana gelir. Bu glikolizin son önemli reaksiyonudur. Piruvatın enol formunun piruvata izomerizasyonu enzimatik olmayan bir şekilde gerçekleşir.
Kuruluşundan bu yana F-1.6-bF Yalnızca enerji açığa çıkaran reaksiyonlar meydana gelir 7 Ve 10 ADP'nin substrat fosforilasyonunun meydana geldiği.
Düzenleme glikoliz
Yerel ve genel düzenlemeler var.
Yerel düzenleme, hücre içindeki çeşitli metabolitlerin etkisi altında enzimlerin aktivitesinin değiştirilmesiyle gerçekleştirilir.
Glikolizin bir bütün olarak düzenlenmesi, tüm organizma için hemen, ikincil habercilerin molekülleri aracılığıyla etkilenerek hücre içi metabolizmayı değiştiren hormonların etkisi altında gerçekleşir.
İnsülin glikolizin uyarılmasında önemli bir rol oynar. Glukagon ve adrenalin glikolizin en önemli hormonal inhibitörleridir.
İnsülin glikolizi aşağıdaki yollarla uyarır:
· heksokinaz reaksiyonunun aktivasyonu;
· fosfofruktokinazın uyarılması;
· piruvat kinazın uyarılması.
Diğer hormonlar da glikolizi etkiler. Örneğin somatotropin glikolitik enzimleri inhibe eder ve tiroid hormonları uyarıcıdır.
Glikoliz birkaç temel adımla düzenlenir. Heksokinaz tarafından katalize edilen reaksiyonlar ( 1 ), fosfofruktokinaz ( 3 ) ve piruvat kinaz ( 10 ) serbest enerjide önemli bir azalma ile karakterize edilir ve pratik olarak geri döndürülemezdir, bu da onların glikolizin etkili düzenleme noktaları olmalarını sağlar.
Glikoliz olağanüstü öneme sahip bir katabolik yoldur. Protein sentezi de dahil olmak üzere hücresel reaksiyonlar için enerji sağlar. Yağların sentezinde glikolizin ara ürünleri kullanılır. Piruvat aynı zamanda alanin, aspartat ve diğer bileşikleri sentezlemek için de kullanılabilir. Glikoliz sayesinde mitokondriyal performans ve oksijen mevcudiyeti, kısa süreli aşırı yükler sırasında kas gücünü sınırlamaz.
2.1.2 Oksidatif dekarboksilasyon - piruvatın asetil-CoA'ya oksidasyonu, piruvat dehidrojenaz kompleksi adı verilen çoklu enzim sisteminde yapısal olarak birleştirilmiş bir dizi enzim ve koenzimin katılımıyla gerçekleşir.
Bu işlemin I. aşamasında piruvat, piruvat dehidrojenaz (E1) enziminin aktif merkezindeki tiamin pirofosfat (TPP) ile etkileşimin bir sonucu olarak karboksil grubunu kaybeder. Aşama II'de, E1-TPP-CHOH-CH3 kompleksinin oksietil grubu, bir asetil grubu oluşturmak üzere oksitlenir ve bu, aynı anda dihidrolipoilasetiltransferaz (E2) enzimiyle ilişkili lipoik asit amide (koenzim) aktarılır. Bu enzim, yüksek enerjili (makroerjik) bir bileşik olan nihai ürün asetil-CoA'nın oluşumuyla asetil grubunun koenzim CoA'ya (HS-KoA) aktarılması olan aşama III'ü katalize eder.
Aşama IV'te, lipoamidin oksitlenmiş formu, indirgenmiş dihidrolipoamid-E2 kompleksinden yeniden üretilir. Dihidrolipoil dehidrojenaz (E3) enziminin katılımıyla hidrojen, dihidrolipoamidin indirgenmiş sülfhidril gruplarından, bu enzimin protez grubu olarak görev yapan ve ona sıkı bir şekilde bağlanan FAD'ye aktarılır. Aşama V'te, indirgenmiş FADH2 dihidro-lipoil dehidrojenaz, NADH + H + oluşturmak üzere hidrojeni koenzim NAD'ye aktarır.
Piruvatın oksidatif dekarboksilasyonu süreci mitokondriyal matriste meydana gelir. (Karmaşık bir çoklu enzim kompleksinin parçası olarak) 3 enzim (piruvat dehidrojenaz, dihidrolipoil asetiltransferaz, dihidrolipoil dehidrojenaz) ve 5 koenzim (TPF, lipoik asit amid, koenzim A, FAD ve NAD) içerir; bunlardan üçü nispeten sıkı bir şekilde enzimlerle ilişkilidir. (TPF-E 1, lipoamid-E 2 ve FAD-E 3) ve ikisi kolayca ayrışır (HS-KoA ve NAD).
Pirinç. 1 Piruvat dehidrojenaz kompleksinin etki mekanizması
E1 - piruvat dehidrojenaz; E2-di-hidrolipoilasetiltransferaz; E3 - dihidrolipoil dehidrojenaz; Dairelerdeki sayılar sürecin aşamalarını göstermektedir.
Alt birim yapısına sahip olan bu enzimlerin tümü ve koenzimler tek bir kompleks halinde organize edilmiştir. Bu nedenle ara ürünler birbirleriyle hızlı bir şekilde etkileşime girebilmektedir. Kompleksi oluşturan dihidrolipoil asetiltransferaz alt birimlerinin polipeptit zincirlerinin, çevresinde piruvat dehidrojenaz ve dihidrolipoil dehidrojenazın yer aldığı kompleksin çekirdeğini oluşturduğu gösterilmiştir. Doğal enzim kompleksinin kendiliğinden birleşmeyle oluştuğu genel olarak kabul edilir.
Piruvat dehidrojenaz kompleksi tarafından katalize edilen genel reaksiyon aşağıdaki gibi temsil edilebilir:
Piruvat + NAD + + HS-CoA - > Asetil-CoA + NADH + H + + CO 2.
Reaksiyona standart serbest enerjide önemli bir azalma eşlik eder ve pratik olarak geri döndürülemez.
Oksidatif dekarboksilasyon sırasında oluşan asetil-CoA, CO2 ve H20 oluşumuyla daha fazla oksidasyona uğrar. Asetil-CoA'nın tam oksidasyonu, trikarboksilik asit döngüsünde (Krebs döngüsü) meydana gelir. Bu işlem, piruvatın oksidatif dekarboksilasyonunun yanı sıra hücrelerin mitokondrisinde meydana gelir.
2 .1.3 DöngütrikarbonikekşiT (döngü Crebsa, kanunkalın döngü) karbonhidratların, yağların ve proteinlerin parçalanması sırasında canlı organizmalarda ara ürünler olarak oluşan iki ve üç karbonlu bileşiklerin CO2'ye dönüştürüldüğü döngüsel bir biyokimyasal aerobik süreç olan genel katabolizma yolunun merkezi parçasıdır. Bu durumda, salınan hidrojen, evrensel enerji kaynağı olan ATP'nin sentezine doğrudan katılarak suya daha da oksitlendiği doku solunum zincirine gönderilir.
Krebs döngüsü, vücuttaki birçok metabolik yolun kesiştiği, oksijen kullanan tüm hücrelerin solunumunda önemli bir adımdır. Önemli enerji rolüne ek olarak, döngü aynı zamanda önemli bir plastik fonksiyona da sahiptir, yani diğer biyokimyasal dönüşümler sırasında hücrenin yaşamı için önemli olan bileşiklerin sentezlendiği önemli bir öncü molekül kaynağıdır. Amino asitler, karbonhidratlar, yağ asitleri vb.
Dönüşüm döngüsü limonasitler canlı hücrelerde keşfedildi ve Alman biyokimyacı Sir Hans Krebs tarafından incelendi, bu çalışmasıyla kendisine (F. Lipman ile birlikte) Nobel Ödülü (1953) verildi.
Ökaryotlarda, Krebs döngüsünün tüm reaksiyonları mitokondri içinde meydana gelir ve bunları katalize eden enzimler, biri hariç, mitokondriyal matriste, iç mitokondriyal membranda lokalize olan süksinat dehidrojenaz hariç, mitokondriyal matriste serbest durumdadır. lipit çift katmanı. Prokaryotlarda döngünün reaksiyonları sitoplazmada gerçekleşir.
Krebs döngüsünün bir devrinin genel denklemi şöyledir:
Asetil-CoA > 2CO2 + CoA + 8e ?
Düzenleme döngüA:
Krebs döngüsü "negatif bir geri besleme mekanizması ile" düzenlenir; büyük miktarda substratın (asetil-CoA, oksaloasetat) varlığında, döngü aktif olarak çalışır ve fazla miktarda reaksiyon ürünü (NAD, ATP) olduğunda, engellenir. Düzenleme aynı zamanda hormonların yardımıyla da gerçekleştirilir; asetil-CoA'nın ana kaynağı glikozdur, bu nedenle glikozun aerobik parçalanmasını destekleyen hormonlar Krebs döngüsünün işleyişine katkıda bulunur. Bu hormonlar şunlardır:
· insülin;
· adrenalin.
Glukagon glukoz sentezini uyarır ve Krebs döngüsü reaksiyonlarını inhibe eder.
Kural olarak, Krebs döngüsünün çalışması, döngüyü substratlarla dolduran anaplerotik reaksiyonlar nedeniyle kesintiye uğramaz:
Piruvat + C02 + ATP = Oksaloasetat (Krebs Döngüsü substratı) + ADP + Fn.
İş ATP sentezleri
Oksidatif fosforilasyon işlemi, 5 tipte 9 alt birimden oluşan mitokondriyal solunum zincirinin beşinci kompleksi - Proton ATP sentaz tarafından gerçekleştirilir:
3 alt birim (d,e,f) ATP sentazının bütünlüğüne katkıda bulunur
· Bir alt birim temel işlevsel birimdir. 3 şekli vardır:
· L-konformasyonu - ADP ve Fosfatı bağlar (özel taşıyıcılar kullanarak sitoplazmadan mitokondriye girer)
T-konformasyonu - fosfat ADP'ye katılır ve ATP oluşur
· O-konformasyonu - ATP, b-alt ünitesinden ayrılır ve b-alt ünitesine aktarılır.
· Bir alt birimin konformasyonunu değiştirebilmesi için bir hidrojen protonu gerekir, konformasyonu 3 kez değiştiği için 3 hidrojen protonu gerekir. Protonlar, elektrokimyasal potansiyelin etkisi altında mitokondrinin zarlar arası boşluğundan pompalanır.
· b-alt birimi, ATP'yi, ATP'yi sitoplazmaya "atan" membran taşıyıcıya taşır. Buna karşılık aynı taşıyıcı ADP'yi sitoplazmadan taşır. Mitokondrinin iç zarı ayrıca sitoplazmadan mitokondriye kadar bir Fosfat taşıyıcısı içerir, ancak bunun çalışması için bir hidrojen protonu gereklidir. Bu tür taşıyıcılara translokazlar denir.
Toplam çıkış
1 ATP molekülünün sentezlenmesi için 3 proton gereklidir.
İnhibitörler oksidatif fosforilasyon
İnhibitörler V kompleksini bloke eder:
· Oligomisin – ATP sentazın proton kanallarını bloke eder.
· Atractylosid, siklofilin – blok translokazlar.
Ayırıcılar oksidatif fosforilasyon
Ayırıcılar- Protonları kabul edebilen ve bunları V kompleksini (proton kanalı) atlayarak mitokondrinin iç zarından aktarabilen lipofilik maddeler. Ayırıcılar:
· Doğal- lipid peroksidasyon ürünleri, uzun zincirli yağ asitleri; yüksek dozda tiroid hormonu.
· Yapay- dinitrofenol, eter, K vitamini türevleri, anestezikler.
2.2 Substrat fosforilasyonu
Yüzey A kesinfosforil Ve fitil ( biyokimyasal), glikolizin redoks reaksiyonlarının enerjisine bağlı olarak (fosfogliseraldehit dehidrojenaz ve enolaz tarafından katalize edilir) ve trikarboksilik asit döngüsünde a-ketoglutarik asidin oksidasyonu sırasında (a-ketoglutarat dehidrojenazın etkisi altında) enerji açısından zengin fosfor bileşiklerinin sentezi. ve süksinat tiyokinaz). Bakteriler için S. f. vakaları tanımlanmıştır. pirüvik asidin oksidasyonu sırasında.C. f., elektron taşıma zincirindeki fosforilasyonun aksine, zehirlerin (örneğin dinitrofenol) "ayrılması" ile inhibe edilmez ve enzimlerin mitokondriyal membranlarda sabitlenmesiyle ilişkili değildir. S. f.'nin katkısı Aerobik koşullar altında hücresel ATP havuzuna katkı, elektron taşıma zincirindeki fosforilasyonun katkısından önemli ölçüde daha azdır.
Bölüm 3. ATP'yi kullanma yolları
3.1 Hücredeki rol
ATP'nin vücuttaki ana rolü, çok sayıda biyokimyasal reaksiyon için enerji sağlamakla ilişkilidir. ATP, iki yüksek enerjili bağın taşıyıcısı olarak, enerji tüketen birçok biyokimyasal ve fizyolojik süreç için doğrudan bir enerji kaynağı görevi görür. Bütün bunlar vücuttaki karmaşık maddelerin sentezinin reaksiyonlarıdır: zar ötesi bir elektrik potansiyelinin oluşturulması da dahil olmak üzere moleküllerin biyolojik zarlar yoluyla aktif transferinin uygulanması; kas kasılmasının uygulanması.
Canlı organizmaların biyoenerjisinde bilindiği gibi iki temel nokta önemlidir:
a) kimyasal enerji, organik substratların oksidasyonunun ekzergonik katabolik reaksiyonlarıyla birlikte ATP oluşumu yoluyla depolanır;
b) kimyasal enerji, anabolizmanın endergonik reaksiyonları ve enerji gerektiren diğer işlemlerle birlikte ATP'nin parçalanması yoluyla kullanılır.
ATP molekülünün biyoenerjetikteki merkezi rolünü neden yerine getirdiği sorusu ortaya çıkıyor. Bunu çözmek için ATP'nin yapısını düşünün Yapı ATP - (en pH 7,0 tetraşarj anyon) .
ATP termodinamik olarak kararsız bir bileşiktir. ATP'nin kararsızlığı, ilk olarak, aynı adı taşıyan bir negatif yük kümesi bölgesindeki elektrostatik itme ile belirlenir, bu da tüm molekülde gerginliğe yol açar, ancak en güçlü bağ P-O-P'dir ve ikinci olarak belirli bir rezonanstır. Son faktöre göre, fosfor atomları arasında, aralarında bulunan oksijen atomunun paylaşılmayan hareketli elektronları için bir rekabet vardır, çünkü her bir fosfor atomu, P=O ve P'nin önemli elektron alıcı etkisinden dolayı kısmi bir pozitif yüke sahiptir. - O- grupları. Dolayısıyla ATP'nin var olma olasılığı, molekülde bu fizikokimyasal stresleri telafi edecek yeterli miktarda kimyasal enerjinin varlığıyla belirlenir. ATP molekülü, hidrolizine serbest enerjide (pH 7.0 ve 37 o C'de) önemli bir azalmanın eşlik ettiği iki fosfoanhidrit (pirofosfat) bağı içerir.
ATP + H20 = ADP + H3PO4G0I = - 31,0 KJ/mol.
ADP + H20 = AMP + H3PO4G0I = - 31,9 KJ/mol.
Biyoenerjinin temel sorunlarından biri, canlı doğada ADP'nin fosforilasyonu yoluyla meydana gelen ATP'nin biyosentezidir.
ADP'nin fosforilasyonu endergonik bir süreçtir ve bir enerji kaynağı gerektirir. Daha önce de belirtildiği gibi, doğada bu tür iki enerji kaynağı hakimdir: güneş enerjisi ve indirgenmiş organik bileşiklerin kimyasal enerjisi. Yeşil bitkiler ve bazı mikroorganizmalar, emilen ışık kuantumunun enerjisini, fotosentezin ışık aşamasında ADP'nin fosforilasyonuna harcanan kimyasal enerjiye dönüştürebilir. Bu ATP yenilenme sürecine fotosentetik fosforilasyon denir. Aerobik koşullar altında organik bileşiklerin oksidasyon enerjisinin ATP'nin makroenerjetik bağlarına dönüşümü esas olarak oksidatif fosforilasyon yoluyla gerçekleşir. ATP oluşumu için gerekli olan serbest enerji, mitokondrinin solunum oksidatif zincirinde üretilir.
Substrat fosforilasyonu adı verilen başka bir ATP sentezi türü bilinmektedir. Elektron transferiyle ilişkili oksidatif fosforilasyonun aksine, ATP rejenerasyonu için gerekli olan aktifleştirilmiş fosforil grubunun (-PO3 H2) donörü, glikoliz işlemlerinin ve trikarboksilik asit döngüsünün ara maddeleridir. Tüm bu durumlarda, oksidatif süreçler yüksek enerjili bileşiklerin oluşumuna yol açar: 1,3-difosfogliserat (glikoliz), süksinil-CoA (trikarboksilik asit döngüsü), uygun enzimlerin katılımıyla ADP'yi yapraklayabilen ve ATP'yi oluşturur. Substrat düzeyinde enerji dönüşümü, anaerobik organizmalarda ATP sentezinin tek yoludur. Bu ATP sentezi süreci, oksijen açlığı dönemlerinde iskelet kaslarının yoğun çalışmasını sürdürmenizi sağlar. Mitokondrisi olmayan olgun kırmızı kan hücrelerinde ATP sentezi için tek yolun bu olduğu unutulmamalıdır.
Hücrenin biyoenerjetiğinde özellikle önemli bir rol, iki fosforik asit kalıntısının bağlandığı adenil nükleotid tarafından oynanır. Bu maddeye adenosin trifosforik asit (ATP) adı verilir. Enerji, ATP molekülünün fosforik asit kalıntıları arasındaki kimyasal bağlarda depolanır ve organik fosforit ayrıldığında açığa çıkar:
ATP= ADP+P+E,
F bir enzimdir, E ise serbest bırakan enerjidir. Bu reaksiyonda, ATP molekülünün geri kalanı ve organik fosfat olan adenosin fosforik asit (ADP) oluşur. Tüm hücreler ATP enerjisini biyosentez işlemleri, hareket, ısı üretimi, sinir uyarıları, lüminesans (örneğin ışıldayan bakteriler), yani tüm hayati süreçler için kullanır.
ATP evrensel bir biyolojik enerji akümülatörüdür. Tüketilen gıdanın içerdiği ışık enerjisi ATP moleküllerinde depolanır.
Hücredeki ATP arzı azdır. Yani kastaki ATP rezervi 20-30 kasılma için yeterlidir. Yoğun ancak kısa süreli çalışma sırasında kaslar yalnızca içerdikleri ATP'nin parçalanması nedeniyle çalışır. İşi bitirdikten sonra kişi ağır nefes alır - bu süre zarfında karbonhidratlar ve diğer maddeler parçalanır (enerji birikir) ve hücrelere ATP temini yeniden sağlanır.
ATP'nin sinapslarda verici olarak rolü de bilinmektedir.
3.2 Enzim fonksiyonundaki rol
Canlı hücre, dengeden uzak bir kimyasal sistemdir; sonuçta canlı bir sistemin dengeye yaklaşması, onun parçalanması ve ölümü anlamına gelir. Her bir enzimin ürünü, metabolik yolda başka bir enzim tarafından substrat olarak kullanıldığı için genellikle hızlı bir şekilde tüketilir. Daha da önemlisi, çok sayıda enzimatik reaksiyon ATP'nin ADP ve inorganik fosfata parçalanmasını içerir. Bunun mümkün olabilmesi için ATP havuzunun dengeden uzak bir seviyede tutulması gerekir, böylece ATP konsantrasyonunun hidroliz ürünlerinin konsantrasyonuna oranı yüksek olur. Böylece ATP havuzu, enzimlerin varlığıyla belirlenen metabolik yollar boyunca enerjinin ve atomların hücreye sürekli aktarımını sağlayan bir "pil" rolünü oynar.
Öyleyse ATP hidroliz sürecini ve bunun enzimlerin işleyişi üzerindeki etkisini ele alalım. İki monomerin (A ve B) suyun salınmasıyla birlikte bir dehidrasyon reaksiyonunda (yoğunlaşma da denir) birbiriyle birleşmesi gereken tipik bir biyosentetik süreci hayal edelim:
A - N + B - OH - AB + H2O
Bir su molekülünün kovalent olarak bağlı A - B bileşiğini parçaladığı hidroliz adı verilen ters reaksiyon, neredeyse her zaman enerji açısından uygun olacaktır. Bu, örneğin proteinlerin, nükleik asitlerin ve polisakkaritlerin alt birimlere hidrolitik parçalanması sırasında meydana gelir.
A - B hücrelerinin A - H ve B - OH ile oluşturulduğu genel strateji, çok aşamalı bir reaksiyon dizisini içerir, bunun sonucunda n Gerekli bileşiklerin enerjik olarak elverişsiz sentezinin dengeli bir faydalı reaksiyonla bağlanması meydana gelir.
ATP hidrolizi büyük bir negatif değere karşılık mı geliyor? G, bu nedenle, ATP hidrolizi, hücre içi biyosentez reaksiyonlarının gerçekleştirilmesinden dolayı sıklıkla enerji açısından uygun bir reaksiyonun rolünü oynar.
ATP hidrolizi ile ilişkili A - H ve B - OH - A - B yolunda, hidroliz enerjisi önce B - OH'yi yüksek enerjili bir ara maddeye dönüştürür, bu daha sonra doğrudan A - H ile reaksiyona girerek A - B'yi oluşturur. Bu işlem için basit bir mekanizma, B - OPO 3 veya B - O - P oluşumuyla fosfatın ATP'den B - OH'ye transferini içerir ve bu durumda toplam reaksiyon yalnızca iki aşamada gerçekleşir:
1) B - OH + ATP - B - B - P + ADP
2) A - N + B - O - R - A - B + R
Reaksiyon sırasında oluşan B - O - P ara bileşiği tekrar yok edildiğinden, genel reaksiyonlar aşağıdaki denklemler kullanılarak açıklanabilir:
3) A-N + B - OH - A - B ve ATP - ADP + P
Enerji açısından uygun olmayan ilk reaksiyonun mümkün olduğu ortaya çıkıyor çünkü enerji açısından uygun olan ikinci reaksiyonla (ATP hidrolizi) ilişkilidir. Bu tip birleşik biyosentetik reaksiyonların bir örneği, amino asit glutaminin sentezidir.
ATP'nin ADP'ye ve inorganik fosfata hidrolizinin G değeri, reaksiyona giren tüm maddelerin konsantrasyonuna bağlıdır ve genellikle hücre koşulları için - 11 ila - 13 kcal / mol aralığında yer alır. ATP hidroliz reaksiyonu son olarak, tabii ki uygun bir reaksiyon dizisinin varlığında, yaklaşık +10 kcal/mol G değeri ile termodinamik açıdan uygun olmayan bir reaksiyonu gerçekleştirmek için kullanılabilir. Ancak birçok biyosentez reaksiyonu için bu bile yetersiz midir? G = - 13 kcal/mol. Bu ve diğer durumlarda ATP hidroliz yolu, önce AMP ve PP'nin (pirofosfat) oluşmasını sağlayacak şekilde değiştirilir. Bir sonraki aşamada pirofosfat da hidrolize uğrar; tüm sürecin toplam serbest enerji değişimi yaklaşık olarak - 26 kcal/mol'dür.
Biyosentetik reaksiyonlarda pirofosfatın hidrolizinden elde edilen enerji nasıl kullanılır? Yollardan biri, A - B bileşiğinin A - H ve B - OH ile yukarıdaki sentezi örneğiyle gösterilebilir. Uygun enzimin yardımıyla B - OH, ATP ile reaksiyona girebilir ve yüksek enerjili B - O - P - P bileşiğine dönüşebilir. Artık reaksiyon üç aşamadan oluşur:
1) B - OH + ATP - B - B - P - P + AMP
2) A - N + B - O - R - R - A - B + RR
3) PP + H2O - 2P
Toplam reaksiyon aşağıdaki gibi temsil edilebilir:
A - H + B - OH - A - B ve ATP + H2O - AMP + 2P
Enzim, katalize edilen reaksiyonu her zaman hem ileri hem de geri yönde hızlandırdığından, A - B bileşiği pirofosfat ile reaksiyona girerek ayrışabilir (reaksiyon, adım 2'nin tersi). Bununla birlikte, pirofosfat hidrolizinin enerji açısından uygun reaksiyonu (adım 3), pirofosfat konsantrasyonunu çok düşük tutarak A-B bileşiğinin stabilitesinin korunmasına yardımcı olur (bu, adım 2'deki ters reaksiyonun oluşmasını önler). Böylece pirofosfat hidrolizinin enerjisi reaksiyonun ileri yönde ilerlemesini sağlar. Bu tip önemli bir biyosentetik reaksiyonun örneği polinükleotidlerin sentezidir.
3.3 DNA, RNA ve proteinlerin sentezindeki rol
Bilinen tüm organizmalarda, DNA'yı oluşturan deoksiribonükleotidler, ribonükleotid redüktaz (RNR) enzimlerinin ilgili ribonükleotidler üzerindeki etkisi ile sentezlenir. Bu enzimler, 2" hidroksil gruplarından, ribonükleosit difosfat substratlarından ve deoksiribonükleosit difosfat ürünlerinden oksijeni uzaklaştırarak şeker kalıntısı oriboz'u deoksiriboz'a indirger. Tüm redüktaz enzimleri, disülfit bağları oluşturmak üzere oksitlenen reaktif sistein kalıntılarına bağlı ortak bir sülfhidril radikal mekanizması kullanır. reaksiyon sırasında PHP enzimi tioredoksin veya glutaredoksin ile reaksiyona sokularak işlenir.
RHP ve ilgili enzimlerin düzenlenmesi birbiriyle ilişkili bir denge sağlar. Çok düşük bir konsantrasyon, DNA sentezini ve DNA onarımını engeller ve hücre için öldürücüdür; anormal bir oran ise, DNA sentezi işlemi sırasında DNA polimerazın birleşme olasılığının artması nedeniyle mutajeniktir.
RNA nükleik asitlerinin sentezi sırasında ATP'den türetilen adenosin, RNA polimeraz tarafından doğrudan RNA moleküllerine katılan dört nükleotidden biridir. Enerji, bu polimerizasyon pirofosfatın (iki fosfat grubu) ortadan kaldırılmasıyla gerçekleşir. Bu süreç, DNA biyosentezinde benzerdir ancak ATP, DNA'ya dahil edilmeden önce deoksiribonükleotid dATP'ye indirgenir.
İÇİNDE sentez sincap. Aminoasil-tRNA sentetazları, bir tRNA molekülünü spesifik amino asidine bağlamak için ATP enzimlerini bir enerji kaynağı olarak kullanır ve ribozomlara transfere hazır bir aminoasil-tRNA oluşturur. Enerji, ATP'nin iki fosfat grubunu ortadan kaldıran adenozin monofosfat (AMP) tarafından hidrolizi yoluyla elde edilebilir.
ATP, maddelerin hücre zarları boyunca taşınması işi de dahil olmak üzere birçok hücresel fonksiyon için kullanılır. Aynı zamanda kas kasılması için gerekli enerjiyi sağlayan mekanik işlerde de kullanılır. Sadece kalp kasına (kan dolaşımı için) ve iskelet kaslarına (örneğin, genel vücut hareketi için) değil, aynı zamanda birçok işlevini yerine getirebilmeleri için kromozomlara ve flagellalara da enerji sağlar. ATP'nin ana rolü, bir hücrenin var olması gereken birkaç bin çeşit makromolekülün sentezi için gerekli enerjiyi sağlayan kimyasal çalışmadır.
ATP aynı zamanda hem kimyasal reaksiyonları kontrol etmek hem de bilgi göndermek için açma-kapama anahtarı olarak da kullanılır. Yaşamda kullanılan yapı taşlarını ve diğer yapıları üreten protein zincirlerinin şekli, öncelikle kolayca kırılabilen ve yeniden yapılandırılabilen zayıf kimyasal bağlar tarafından belirlenir. Bu devreler enerji giriş veya çıkışına yanıt olarak kısaltılabilir, uzatılabilir ve şekil değiştirebilir. Zincirlerdeki değişiklikler proteinin şeklini değiştirdiği gibi fonksiyonunu da değiştirebilir veya aktif ya da pasif hale gelmesine neden olabilir.
ATP molekülleri, bir protein molekülünün bir kısmına bağlanabilir, bu da aynı molekülün başka bir kısmının kaymasına veya hafifçe hareket etmesine neden olur, bu da onun konformasyonunu değiştirmesine ve molekülün etkisiz hale gelmesine neden olur. ATP uzaklaştırıldıktan sonra proteinin orijinal formuna dönmesine neden olur ve böylece tekrar işlevsel hale gelir.
Döngü, molekül geri dönene kadar tekrarlanabilir ve etkili bir şekilde hem açma/kapama düğmesi görevi görür. Hem fosforun eklenmesi (fosforilasyon) hem de bir proteinden fosforun uzaklaştırılması (defosforilasyon), bir açma veya kapama anahtarı görevi görebilir.
3.4 ATP'nin diğer işlevleri
Rol V metabolizma, sentez Ve aktif Ulaşım
Böylece ATP, mekansal olarak ayrılmış metabolik reaksiyonlar arasında enerji aktarır. ATP çoğu hücresel fonksiyon için ana enerji kaynağıdır. Bu, DNA ve RNA dahil olmak üzere makromoleküllerin ve proteinlerin sentezini içerir. ATP ayrıca ekzositoz ve endositoz gibi makromoleküllerin hücre zarlarından taşınmasında da önemli bir rol oynar.
Rol V yapı hücreler Ve hareket
ATP, hücre iskeleti elemanlarının birleştirilmesini ve sökülmesini kolaylaştırarak hücresel yapının korunmasında rol oynar. Bu işlem nedeniyle aktin filamentlerinin kasılması için ATP, kas kasılması için ise miyozin gereklidir. Bu son süreç hayvanların temel enerji gereksinimlerinden biridir ve hareket ve solunum için gereklidir.
Rol V sinyal sistemler
İçindehücre dışısinyalsistemler
ATP aynı zamanda bir sinyal molekülüdür. ATP, ADP veya adenozin purinerjik reseptörler olarak tanınır. Purinoreseptörler memeli dokularında en fazla bulunan reseptörler olabilir.
İnsanlarda bu sinyal verme rolü hem merkezi hem de çevresel sinir sistemlerinde önemlidir. Aktivite, membran reseptörlerinin purinerjik aktivasyonu yoluyla sinapslardan, aksonlardan ve glialardan ATP salınmasına bağlıdır.
İçindehücre içisinyalsistemler
ATP, sinyal iletim süreçlerinde kritik öneme sahiptir. Kinazlar tarafından fosfat transfer reaksiyonlarında fosfat grubu kaynağı olarak kullanılır. Membran proteinleri veya lipidler gibi destekler üzerindeki kinazlar yaygın bir sinyal biçimidir. Kinazlarla protein fosforilasyonu, mitojenle aktifleştirilen protein kinaz kademesi gibi bu kademeyi aktive edebilir.
ATP aynı zamanda adenilat siklaz tarafından da kullanılır ve hücre içi depolardan kalsiyumun salınması için kalsiyum sinyallerinin tetiklenmesinde rol oynayan AMP adı verilen ikinci bir haberci moleküle dönüştürülür. [38] Bu sinyal formu, diğer birçok hücresel sürecin düzenlenmesinde yer almasına rağmen, beyin fonksiyonunda özellikle önemlidir.
Çözüm
1. Adenozin trifosfat - bir nükleotid, organizmalarda enerji ve madde alışverişinde son derece önemli bir rol oynar; Her şeyden önce bileşiğin, canlı sistemlerde meydana gelen tüm biyokimyasal süreçler için evrensel bir enerji kaynağı olduğu bilinmektedir. Kimyasal olarak ATP, adenin ve ribozun bir türevi olan adenosinin trifosfat esteridir. ATP'nin yapısı RNA'nın bir parçası olan adenin nükleotidine benzer, ancak bir fosforik asit yerine ATP üç fosforik asit kalıntısı içerir. Hücreler gözle görülür miktarlarda asitleri değil, yalnızca tuzlarını içerebilir. Bu nedenle fosforik asit ATP'ye bir kalıntı olarak girer (asitin OH grubu yerine negatif yüklü bir oksijen atomu vardır).
2. Vücutta ATP, ADP'nin fosforilasyonuyla sentezlenir:
ADP + H3PO4 + enerji> ATP + H 2 O.
ADP'nin fosforilasyonu iki şekilde mümkündür: substrat fosforilasyonu ve oksidatif fosforilasyon (oksitleyici maddelerin enerjisini kullanarak).
Oksidatif fosforilasyon - ATP formunda enerji üretimine yol açan hücresel solunumun en önemli bileşenlerinden biri. Oksidatif fosforilasyonun substratları, organik bileşiklerin (proteinler, yağlar ve karbonhidratlar) parçalanma ürünleridir. Oksidatif fosforilasyon süreci mitokondrinin kristalarında gerçekleşir.
Yüzey A kesinfosforil Ve fitil ( biyokimyasal), glikolizin redoks reaksiyonlarının enerjisine bağlı olarak ve trikarboksilik asit döngüsünde a-ketoglutarik asidin oksidasyonu sırasında enerji açısından zengin fosfor bileşiklerinin sentezi.
3. ATP'nin vücuttaki ana rolü, çok sayıda biyokimyasal reaksiyon için enerji sağlamakla ilişkilidir. ATP, iki yüksek enerjili bağın taşıyıcısı olarak, enerji tüketen birçok biyokimyasal ve fizyolojik süreç için doğrudan bir enerji kaynağı görevi görür. Canlı organizmaların biyoenerjisinde aşağıdakiler önemlidir: kimyasal enerji, organik substratların oksidasyonunun ekzergonik katabolik reaksiyonlarıyla birlikte ATP oluşumu yoluyla depolanır; Kimyasal enerji, anabolizmanın endergonik reaksiyonları ve enerji harcaması gerektiren diğer işlemlerle birlikte ATP'nin parçalanması yoluyla kullanılır.
4. Artan yük ile (örneğin kısa mesafeli koşularda), kaslar yalnızca ATP tedariki nedeniyle çalışır. Kas hücrelerinde bu rezerv birkaç düzine kasılma için yeterlidir ve ardından ATP miktarının yenilenmesi gerekir. ADP ve AMP'den ATP sentezi, karbonhidratların, lipitlerin ve diğer maddelerin parçalanması sırasında açığa çıkan enerji nedeniyle oluşur. Zihinsel çalışma yapmak aynı zamanda büyük miktarda ATP gerektirir. Bu nedenle zihinsel çalışması olan kişiler, parçalanması ATP sentezini sağlayan artan miktarda glikoza ihtiyaç duyar.
ATP, enerjinin yanı sıra vücutta eşit derecede önemli bir dizi başka işlevi de yerine getirir:
· Diğer nükleozid trifosfatlarla birlikte ATP, nükleik asitlerin sentezinde başlangıç ürünüdür.
· Ayrıca ATP birçok biyokimyasal sürecin düzenlenmesinde önemli rol oynar. Bir dizi enzimin allosterik efektörü olan ATP, düzenleyici merkezlerine katılarak aktivitelerini arttırır veya bastırır.
· ATP aynı zamanda hücreye hormonal sinyal iletiminin ikincil habercisi olan siklik adenosin monofosfatın sentezinin doğrudan öncüsüdür.
ATP'nin sinapslarda verici olarak rolü de bilinmektedir.
Kaynakça
1. Lemeza, N.A. Üniversitelere başvuranlar için biyoloji kılavuzu / L.V. Kamlyuk N.D. Lisov. - Mn .: Unipress, 2011 - 624 s.
2. Lodish, H, Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J. Moleküler Hücre Biyolojisi, 5. baskı. - New York: W. H. Freeman, 2004.
3. Romanovsky, Yu.M. Canlı hücrelerin moleküler enerji dönüştürücüleri. Proton ATP sentaz - dönen bir moleküler motor / Yu.M. Romanovsky A.N. Tikhonov // UFN. - 2010. - T.180. - S.931 - 956.
4. Voet D, Voet JG. Biyokimya Cilt 1 3. baskı. - Wiley: Hoboken, New Jersey. - N-Y: W. H. Freeman and Company, 2002. - 487 ovmak.
5. Genel kimya. Biyofiziksel kimya. Biyojenik elementlerin kimyası. M.: Yüksekokul, 1993
6.Vershubsky, A.V. Biyofizik. / A.V. Vershubsky, V.I. Priklonsky, A.N. Tihonov. - M: 471-481.
7. Alberts B. Hücrelerin moleküler biyolojisi, 3 ciltlik. / Alberts B., Bray D., Lewis J. ve diğerleri M.: Mir, 1994.1558 s.
8. Nikolaev A.Ya. Biyolojik kimya - M .: Medical Information Agency LLC, 1998.
9. Berg, J. M. Biochemistry, uluslararası baskı. / Berg, J.M, Tymoczko, J.L, Stryer, L. - New York: WH Freeman, 2011; s287.
10. Knorre D.G. Biyolojik kimya: Ders Kitabı. kimya için, biyol. Ve tatlım. uzman. üniversiteler - 3. baskı, rev. / Knorre D.G., Mysina S.D. - M.: Daha yüksek. okul, 2000. - 479 s.: hasta.
11. Eliot, V. Biyokimya ve moleküler biyoloji / V. Eliot, D. Eliot. - M .: Rusya Tıp Bilimleri Akademisi Biyomedikal Kimya Araştırma Enstitüsü Yayınevi, LLC "Materik-alpha", 1999, - 372 s.
12. Shina CL, K., 7 Areieh, W. Çözeltideki ATP Hidrolizinin Enerjisi Üzerine. Fiziksel Kimya Dergisi B, 113 (47), (2009).
13. Berg, J.M. Biyokimya / J.M. Berg: J.L. Tymoczko, L. Stryer. - N-Y: W. H. Freeman and Company, 2002. - 1514 s.
...Benzer belgeler
İnsan vücudundaki organik bileşikler. Proteinlerin yapısı, fonksiyonları ve sınıflandırılması. Nükleik asitler (polinükleotitler), RNA ve DNA'nın yapısal özellikleri ve özellikleri. Doğada ve insan vücudunda karbonhidratlar. Lipitler yağlar ve yağ benzeri maddelerdir.
özet, 09/06/2009 eklendi
Protein sentezi süreci ve canlı organizmaların yaşamındaki rolü. Amino asitlerin fonksiyonları ve kimyasal özellikleri. İnsan vücudundaki eksikliklerinin nedenleri. Esansiyel asitleri içeren gıda türleri. Amino asitler karaciğerde sentezlenir.
sunum, 23.10.2014 eklendi
Karbonhidratların enerji, depolama ve destek oluşturma fonksiyonları. İnsan vücudunda ana enerji kaynağı olan monosakkaritlerin özellikleri; glikoz. Disakkaritlerin başlıca temsilcileri; sakaroz. Polisakkaritler, nişasta oluşumu, karbonhidrat metabolizması.
rapor, 30.04.2010 eklendi
Vücuttaki metabolik işlevler: Besinlerin parçalanması sırasında üretilen enerjinin organlara ve sistemlere sağlanması; gıda moleküllerini yapı taşlarına dönüştürmek; nükleik asitlerin, lipitlerin, karbonhidratların ve diğer bileşenlerin oluşumu.
özet, 20.01.2009 eklendi
Tüm hayati süreçlerin normal seyrinde proteinlerin, yağların ve karbonhidratların rolü ve önemi. Proteinlerin, yağların ve karbonhidratların bileşimi, yapısı ve temel özellikleri, bunların vücuttaki en önemli görevleri ve fonksiyonları. Bu besinlerin ana kaynakları.
sunum, 04/11/2013 eklendi
Hücre zarının önemli bir bileşeni olarak kolesterol moleküllerinin yapısının özellikleri. İnsan vücudunda kolesterol metabolizmasının düzenlenme mekanizmalarının incelenmesi. Kan dolaşımında aşırı düşük yoğunluklu lipoproteinlerin ortaya çıkmasının özelliklerinin analizi.
özet, 17.06.2012 eklendi
Proteinlerin, lipitlerin ve karbonhidratların metabolizması. İnsan beslenmesi türleri: omnivor, ayrı ve düşük karbonhidratlı beslenme, vejetaryenlik, çiğ gıda diyeti. Proteinlerin metabolizmadaki rolü. Vücutta yağ eksikliği. Diyet türündeki değişikliklerin bir sonucu olarak vücutta meydana gelen değişiklikler.
kurs çalışması, eklendi 02/02/2014
Demirin oksidatif süreçlere ve kollajen sentezine katılımının dikkate alınması. Kan oluşumu süreçlerinde hemoglobinin öneminin anlaşılması. İnsan vücudunda demir eksikliği sonucu baş dönmesi, nefes darlığı ve metabolik bozukluklar.
sunum, eklendi: 02/08/2012
Flor ve demirin özellikleri. Vücudun günlük ihtiyacı. Florun vücuttaki işlevleri, etkisi, öldürücü dozu, diğer maddelerle etkileşimi. İnsan vücudundaki demir, kaynakları. Vücut ve fazlalığı için demir eksikliğinin sonuçları.
sunum, eklendi: 02/14/2017
Besin kaynağı olarak proteinler, temel işlevleri. Proteinlerin oluşumunda rol oynayan amino asitler. Polipeptit zincirinin yapısı. Vücuttaki proteinlerin dönüşümleri. Tam ve eksik proteinler. Protein yapısı, kimyasal özellikleri, niteliksel reaksiyonlar.
Vücudumuzun herhangi bir hücresinde milyonlarca biyokimyasal reaksiyon meydana gelir. Genellikle enerji gerektiren çeşitli enzimler tarafından katalize edilirler. Hücre bunu nereden alıyor? Ana enerji kaynaklarından biri olan ATP molekülünün yapısını düşünürsek bu soru cevaplanabilir.
ATP evrensel bir enerji kaynağıdır
ATP, adenozin trifosfat veya adenozin trifosfat anlamına gelir. Bu madde herhangi bir hücredeki en önemli iki enerji kaynağından biridir. ATP'nin yapısı ve biyolojik rolü yakından ilişkilidir. Çoğu biyokimyasal reaksiyon yalnızca bir maddenin moleküllerinin katılımıyla gerçekleşebilir, bu özellikle doğrudur, ancak ATP nadiren doğrudan reaksiyona dahil olur: herhangi bir işlemin gerçekleşmesi için, tam olarak adenozin trifosfatta bulunan enerjiye ihtiyaç vardır.
Maddenin moleküllerinin yapısı, fosfat grupları arasında oluşan bağların büyük miktarda enerji taşıyacak şekildedir. Bu nedenle bu tür bağlara makroerjik veya makroenerjetik (makro=çok, çok miktarda) adı da verilir. Terim ilk olarak bilim adamı F. Lipman tarafından tanıtıldı ve ayrıca bunları belirtmek için ̴ sembolünün kullanılmasını önerdi.
Hücrenin sabit bir adenosin trifosfat seviyesini koruması çok önemlidir. Bu özellikle kas dokusu hücreleri ve sinir lifleri için geçerlidir, çünkü bunlar enerjiye en bağımlı olanlardır ve işlevlerini yerine getirmek için yüksek miktarda adenozin trifosfat gerektirirler.
ATP molekülünün yapısı
Adenozin trifosfat üç elementten oluşur: riboz, adenin ve kalıntılar

Riboz- pentoz grubuna ait bir karbonhidrat. Bu, ribozun bir döngü içinde yer alan 5 karbon atomu içerdiği anlamına gelir. Riboz, adenine 1. karbon atomundaki β-N-glikosidik bağ yoluyla bağlanır. Pentoza 5. karbon atomundaki fosforik asit kalıntıları da eklenir.
Adenin azotlu bir bazdır. Riboza hangi azotlu bazın bağlandığına bağlı olarak GTP (guanozin trifosfat), TTP (timidin trifosfat), CTP (sitidin trifosfat) ve UTP (üridin trifosfat) da ayırt edilir. Bu maddelerin tümü yapı olarak adenozin trifosfata benzer ve yaklaşık olarak aynı işlevleri yerine getirir, ancak hücrede çok daha az yaygındırlar.
Fosforik asit kalıntıları. Riboza en fazla üç fosforik asit kalıntısı bağlanabilir. İki veya yalnızca bir tane varsa, maddeye ADP (difosfat) veya AMP (monofosfat) adı verilir. Makroenerjetik bağların oluştuğu fosfor kalıntıları arasında, kopmadan sonra 40 ila 60 kJ enerji açığa çıkar. İki bağ kırılırsa, 80, daha az sıklıkla - 120 kJ enerji açığa çıkar. Riboz ile fosfor kalıntısı arasındaki bağ koptuğunda yalnızca 13,8 kJ açığa çıkar, dolayısıyla trifosfat molekülünde yalnızca iki yüksek enerjili bağ vardır (P ̴ P ̴ P), ADP molekülünde ise bir (P ̴) vardır. P).
Bunlar ATP'nin yapısal özellikleridir. Fosforik asit kalıntıları arasında makroenerjetik bir bağ oluşması nedeniyle ATP'nin yapısı ve fonksiyonları birbirine bağlıdır.
ATP'nin yapısı ve molekülün biyolojik rolü. Adenozin trifosfatın ek fonksiyonları
ATP, enerjinin yanı sıra hücrede birçok başka işlevi de yerine getirebilir. Diğer nükleotid trifosfatlarla birlikte trifosfat, nükleik asitlerin yapımında rol oynar. Bu durumda ATP, GTP, TTP, CTP ve UTP azotlu bazların tedarikçileridir. Bu özellik işlemlerde ve transkripsiyonda kullanılır.
ATP ayrıca iyon kanallarının çalışması için de gereklidir. Örneğin Na-K kanalı, 3 sodyum molekülünü hücre dışına, 2 potasyum molekülünü hücre içine pompalar. Bu iyon akımı, zarın dış yüzeyinde pozitif yükü korumak için gereklidir ve kanal yalnızca adenozin trifosfatın yardımıyla işlev görebilir. Aynı durum proton ve kalsiyum kanalları için de geçerlidir.
ATP, ikinci haberci cAMP'nin (siklik adenozin monofosfat) öncüsüdür - cAMP yalnızca hücre zarı reseptörleri tarafından alınan sinyali iletmekle kalmaz, aynı zamanda allosterik bir efektördür. Allosterik efektörler enzimatik reaksiyonları hızlandıran veya yavaşlatan maddelerdir. Böylece siklik adenozin trifosfat, bakteri hücrelerinde laktozun parçalanmasını katalize eden bir enzimin sentezini inhibe eder.
Adenozin trifosfat molekülünün kendisi de allosterik bir efektör olabilir. Ayrıca, bu tür işlemlerde ADP, ATP'ye karşı bir antagonist görevi görür: eğer trifosfat reaksiyonu hızlandırırsa, difosfat onu inhibe eder ve bunun tersi de geçerlidir. Bunlar ATP'nin işlevleri ve yapısıdır.

ATP hücrede nasıl oluşur?
ATP'nin işlevleri ve yapısı, maddenin moleküllerinin hızla kullanılıp yok edilmesini sağlayacak şekildedir. Bu nedenle trifosfat sentezi hücrede enerji oluşumunda önemli bir süreçtir.
Adenozin trifosfatın sentezi için en önemli üç yöntem vardır:
1. Substrat fosforilasyonu.
2. Oksidatif fosforilasyon.
3. Fotofosforilasyon.
Substrat fosforilasyonu hücre sitoplazmasında meydana gelen çoklu reaksiyonlara dayanır. Bu reaksiyonlara glikoliz - anaerobik aşama denir. 1 glikoliz döngüsü sonucunda 1 molekül glikozdan iki molekül sentezlenir, bunlar daha sonra enerji üretmek için kullanılır ve ayrıca iki ATP de sentezlenir.
- C6H1206 + 2ADP + 2Pn --> 2C3H403 + 2ATP + 4H.
Hücre solunumu
Oksidatif fosforilasyon, elektronların membran elektron taşıma zinciri boyunca aktarılmasıyla adenozin trifosfatın oluşmasıdır. Bu transferin bir sonucu olarak, zarın bir tarafında bir proton gradyanı oluşur ve ATP sentazın protein integral seti yardımıyla moleküller oluşturulur. İşlem mitokondriyal membranda gerçekleşir.

Mitokondrideki glikoliz ve oksidatif fosforilasyonun aşamalarının sırası, solunum adı verilen ortak bir süreci oluşturur. Tam bir döngünün ardından hücredeki 1 glikoz molekülünden 36 ATP molekülü oluşur.
Fotofosforilasyon
Fotofosforilasyon işlemi aynı oksidatif fosforilasyondur ancak tek bir fark vardır: Fotofosforilasyon reaksiyonları, ışığın etkisi altında hücrenin kloroplastlarında meydana gelir. ATP, yeşil bitkilerde, alglerde ve bazı bakterilerde ana enerji üretim süreci olan fotosentezin hafif aşamasında üretilir.
Fotosentez sırasında elektronlar aynı elektron taşıma zincirinden geçerek proton gradyanının oluşmasına neden olur. Membranın bir tarafındaki protonların konsantrasyonu ATP sentezinin kaynağıdır. Moleküllerin montajı ATP sentaz enzimi tarafından gerçekleştirilir.

Ortalama hücre, ağırlıkça %0,04 adenozin trifosfat içerir. Ancak en yüksek değer kas hücrelerinde görülür: %0,2-0,5.
Bir hücrede yaklaşık 1 milyar ATP molekülü vardır.
Her molekül 1 dakikadan fazla yaşamaz.
Bir molekül adenozin trifosfat günde 2000-3000 kez yenilenir.
Toplamda insan vücudu günde 40 kg adenozin trifosfat sentezler ve herhangi bir zamanda ATP rezervi 250 g'dır.

Çözüm
ATP'nin yapısı ve moleküllerinin biyolojik rolü yakından ilişkilidir. Bu madde yaşam süreçlerinde önemli bir rol oynar çünkü fosfat kalıntıları arasındaki yüksek enerjili bağlar büyük miktarda enerji içerir. Adenozin trifosfat hücrede birçok işlevi yerine getirir ve bu nedenle maddenin sabit bir konsantrasyonunu korumak önemlidir. Biyokimyasal reaksiyonlarda bağların enerjisi sürekli kullanıldığı için bozunma ve sentez yüksek hızda meydana gelir. Bu, vücuttaki herhangi bir hücre için gerekli bir maddedir. Muhtemelen ATP'nin yapısı hakkında söylenebilecek tek şey budur.